亘喜生物_亘喜生物科技集团
*** 次数:1999998 已用完,请联系开发者***

ORR达93.1%,亘喜生物ASCO口头报告双靶点CAR-T疗法最新临床数据6月4日,亘喜生物宣布该公司以口头报告形式在2023年美国临床肿瘤学会(ASCO)年会上公布了一项评估B细胞成熟抗原(BCMA)和CD19双靶点自体FasTCAR-T疗法GC012F治疗复发/难治性多发性骨髓瘤(RRMM)的多中心临床研究的长期随访数据。数据显示,患者的总体应答率(ORR)为9...
●﹏●

亘喜生物在2023 ASCO年会上正式公布FasTCAR-T GC012F治疗...上海和美国加利福尼亚州圣迭戈2023年6月4日 /美通社/ -- 亘喜生物科技集团(纳斯达克股票代码:GRCL;简称“亘喜生物” 或“公司”) 是一家面向全球、处于临床阶段的生物制药企业,致力于开发创新、高效的细胞与基因疗法,以治疗癌症及自身免疫性疾病。今日,公司正式以口头报告(摘...
ˇωˇ
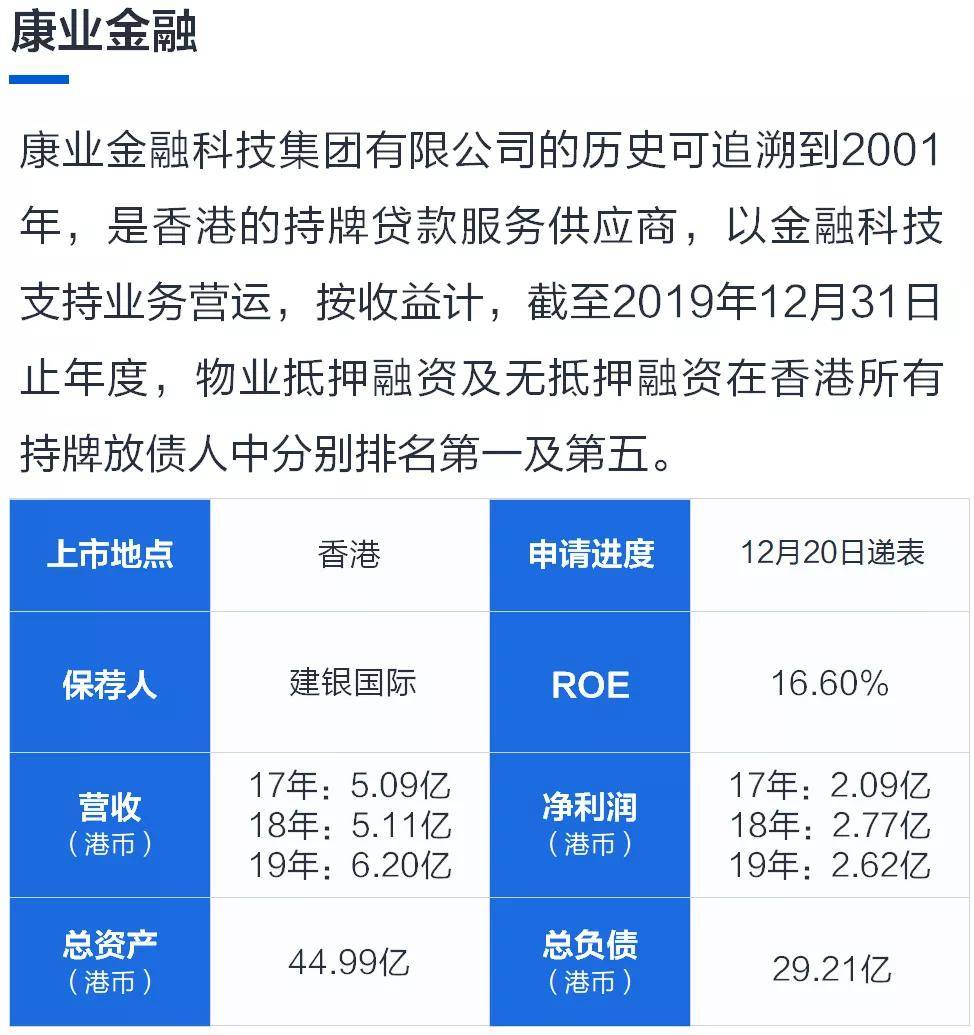
亘喜生物(GRCL.US)Q1净亏损1.517亿元 研发支出增至1.375亿元智通财经APP获悉,5月15日美股盘前,亘喜生物(GRCL.US)公布了2023年第一季度未经审计的财务业绩。财报显示,亘喜生物Q1归属于普通股股东净亏损1.517亿元(人民币,下同),上年同期净亏损为1.586亿元;基本和摊薄后每股亏损为0.45元,上年同期每股亏损为0.47元。一季度,公司研发支...

亘喜生物宣布启动GC012F针对难治性系统性红斑狼疮(SLE)的临床试验亘喜生物宣布启动一项全新的由研究者发起的临床试验(IIT),对FasTCAR-T GC012F的临床探索将扩展至自身免疫性疾病- GC012F开创性地将CD19/BCMA双靶点CAR-T疗法应用于系统性红斑狼疮,旨在更深入、广泛地清除致病性B细胞和浆细胞中国江苏苏州、上海和美国加利福尼亚州...

●^●
亘喜生物(GRCL.US)Q4业绩会议纪要:继续推进与优化GC012F疗法 将...智通财经APP获悉,3月13日(周一)美股盘前,亘喜生物(GRCL.US)公布了2022年第四季度及全年财务业绩。财报显示,亘喜生物Q4归属于普通股股东净亏损1.307亿元(人民币,下同),上年同期净亏损为1.286亿元;基本和摊薄后每股亏损为0.39元,上年同期每股亏损为0.38元。四季度,公司研发...

亘喜生物(GRCL.US)Q4净亏损1.3亿元 研发支出增至1.13亿元智通财经APP获悉,3月13日(周一)美股盘前,亘喜生物(GRCL.US)公布了2022年第四季度及全年财务业绩。财报显示,亘喜生物Q4归属于普通股股东净亏损1.307亿元(人民币,下同),上年同期净亏损为1.286亿元;基本和摊薄后每股亏损为0.39元,上年同期每股亏损为0.38元。四季度,公司研发...
亘喜生物(GRCL.US)将于3月13日美股盘前公布Q4业绩智通财经APP获悉,亘喜生物(GRCL.US)宣布将于3月13日美股盘前公布2022年第四季度财务业绩。同时,公司管理层将于同日北京时间21:00(美东时间8:00)举行业绩电话会议。本文源自智通财经网

亘喜生物(GRCL.US)GC012F疗法新药临床试验申请获中国监管机构批准智通财经APP获悉,2月13日,亘喜生物(GRCL.US)宣布,中国国家药品监督管理局(NMPA)药品审评中心(CDE)正式批准了该公司旗下自体CAR-T候选产品GC012F针对复发/难治性多发性骨髓瘤(RRMM)的新药临床试验(IND)申请。亘喜生物计划于2023年第三季度在中国启动该项单臂、开...
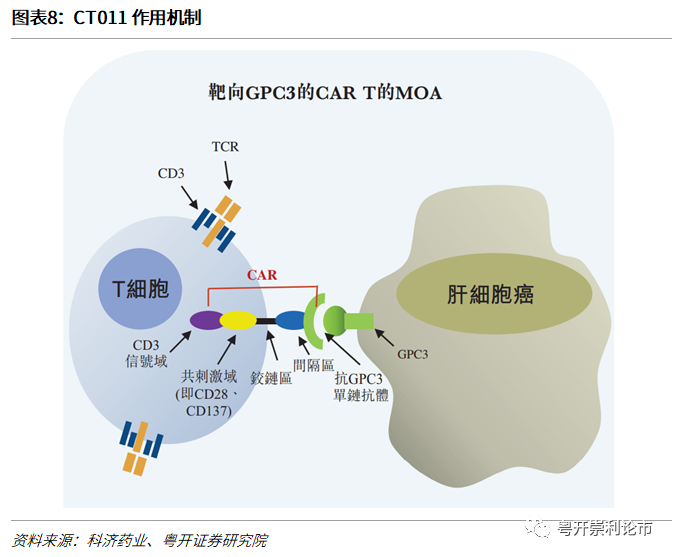
亘喜生物GC012F疗法新药临床试验申请获中国监管机构批准2月13日,亘喜生物宣布,中国国家药品监督管理局(NMPA)药品审评中心(CDE)正式批准了该公司旗下自体CAR-T候选产品GC012F针对复发/难治性多发性骨髓瘤(RRMM)的新药临床试验(IND)申请。亘喜生物计划于2023年第三季度在中国启动该项单臂、开放性、多中心的1/2期临床试验...
亘喜生物治疗急性B淋巴细胞白血病临床试验进入新阶段亘喜生物科技集团宣布正在中国开展的、旨在全面评估GC007g治疗复发/难治性急性B淋巴细胞白血病效果的1/2期注册性临床试验顺利进入2期研究阶段,首例入组患者已给药。GC007g是亘喜生物旗下的一款靶向CD19的供者来源异基因CAR-T细胞疗法,用于治疗接受过同种异体干细胞...
老王加速器部分文章、数据、图片来自互联网,一切版权均归源网站或源作者所有。
如果侵犯了你的权益请来信告知删除。邮箱:xxxxxxx@qq.com
上一篇:亘喜生物科技集团
下一篇:亘喜生物科技有限公司






